Antes de leer: En skinpaths distinguimos opinión de evidencia. Este contenido se basa en literatura médica indexada y recomendaciones de sociedades científicas. Al final encontrarás bibliografía completa para comprobarla y profundizar.
Objetivos de aprendizaje
-
Reconocer en H&E la arquitectura en capas: epidermis → unión dermoepidérmica → dermis → hipodermis.
-
Identificar los estratos epidérmicos y sus “pistas” morfológicas.
-
Entender qué es la zona de membrana basal (unión dermoepidérmica) y por qué importa.
-
Diferenciar dermis papilar vs reticular con criterios reproducibles.
-
Ubicar células clave (queratinocito, melanocito, célula de Langerhans, fibroblasto, adipocito) y su función.
-
Aplicar una lectura sistemática para no perderse ante variaciones normales (sitio anatómico, piel gruesa/delgada, anexos).
Hechos fundacionales (lo que sí o sí debes saber)
-
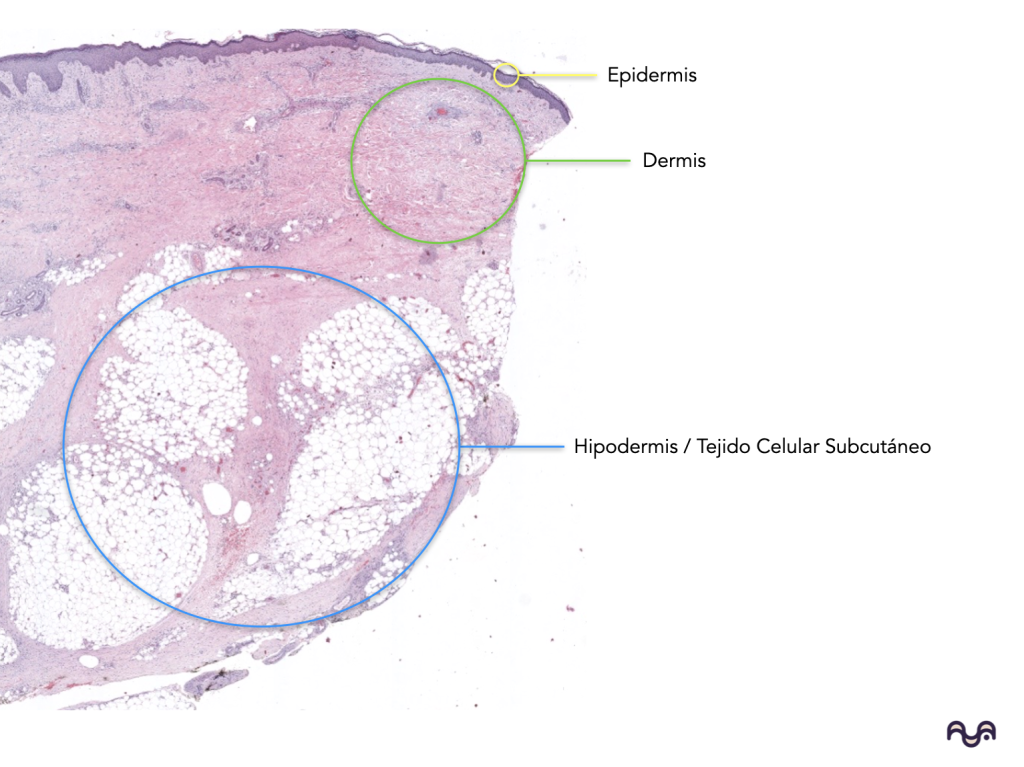
La piel se organiza en epidermis (epitelio estratificado escamoso queratinizado), dermis (tejido conectivo) e hipodermis (tejido adiposo lobulillar con septos). Agarwal 2023
-
La epidermis es avascular; se nutre por difusión desde la dermis a través de la unión dermoepidérmica. Yousef 2024
-
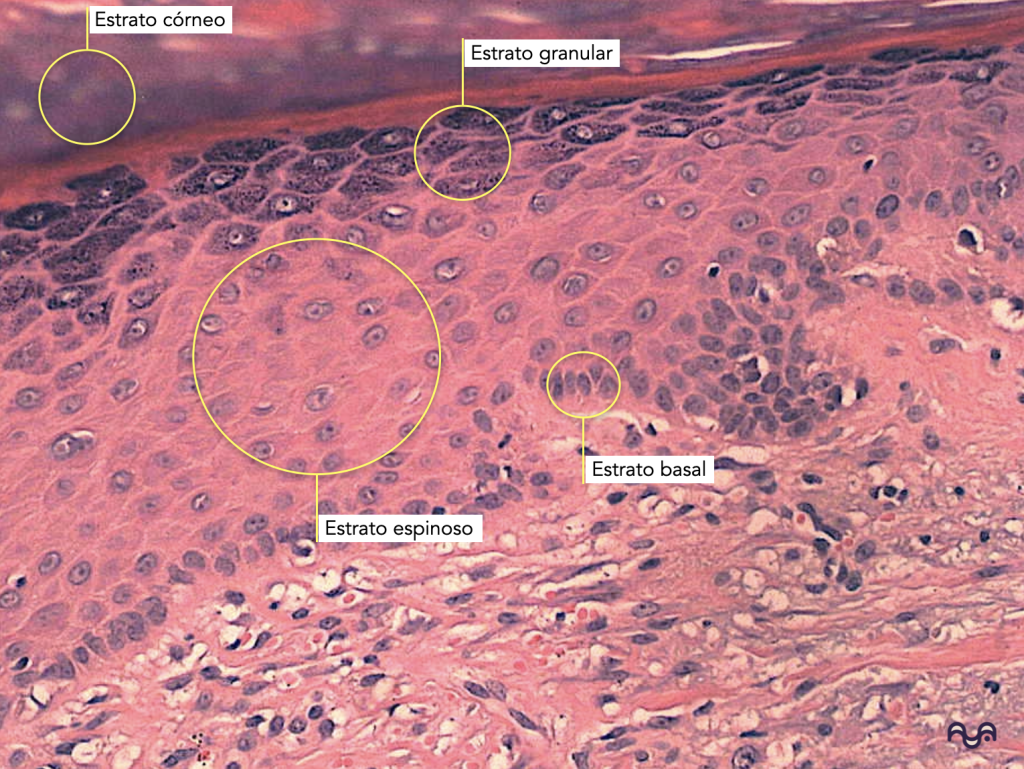
Estratos epidérmicos (superficial → profundo): córneo, granuloso, espinoso, basal.
El estrato lúcido solo presente en piel gruesa (palmas/plantas). Kim 2023
-
En H&E, el estrato granuloso destaca por gránulos basófilos de queratohialina; el estrato espinoso por “puentes intercelulares” (desmosomas).
-
El queratinocito domina la epidermis y completa la cornificación para formar el estrato córneo (barrera física). Gutowska-Owsiak 2020
-
La barrera del estrato córneo se entiende como “ladrillos y mortero”: corneocitos (ladrillos) + lípidos lamelares (mortero). Del Rosso 2016
-
La unión dermoepidérmica (zona de membrana basal) es una suprastructura de adhesión; su integridad depende de laminina-332, colágeno IV, perlecano, e interacciones con integrinas/hemidesmosomas. Kiritsi 2013, Behrens 2012
-
Los filamentos de anclaje y las fibrillas de anclaje (colágeno VII) conectan epidermis con dermis papilar: “zona crítica” para ampollas subepidérmicas. Goletz 2017, Villone 2008
-
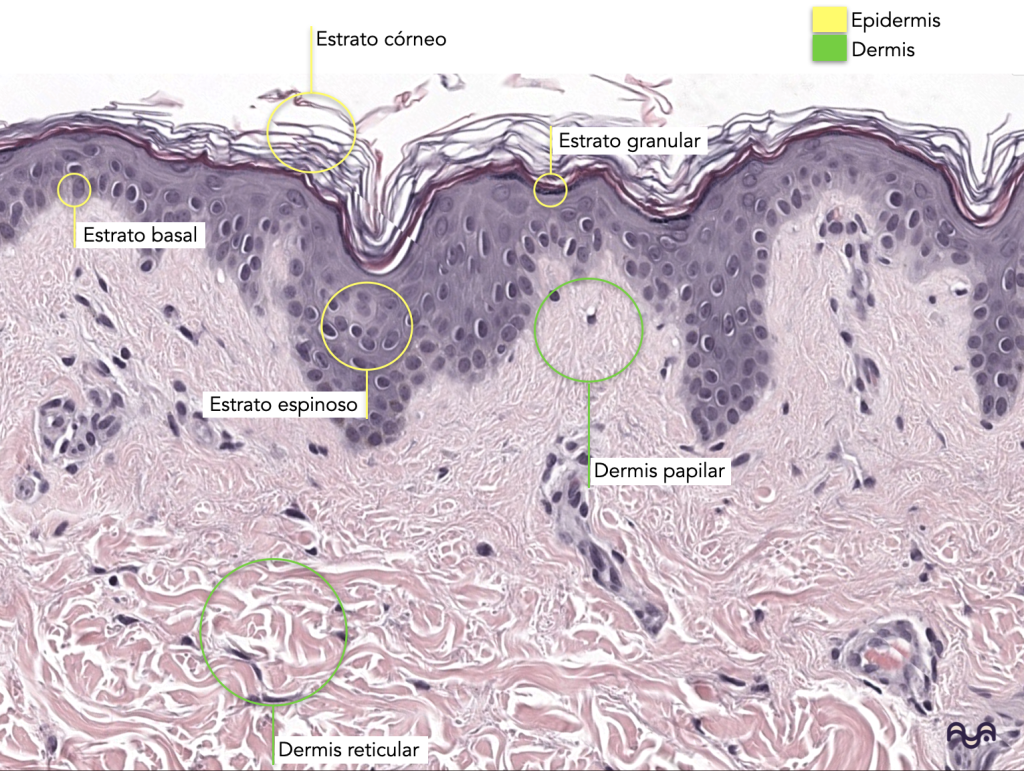
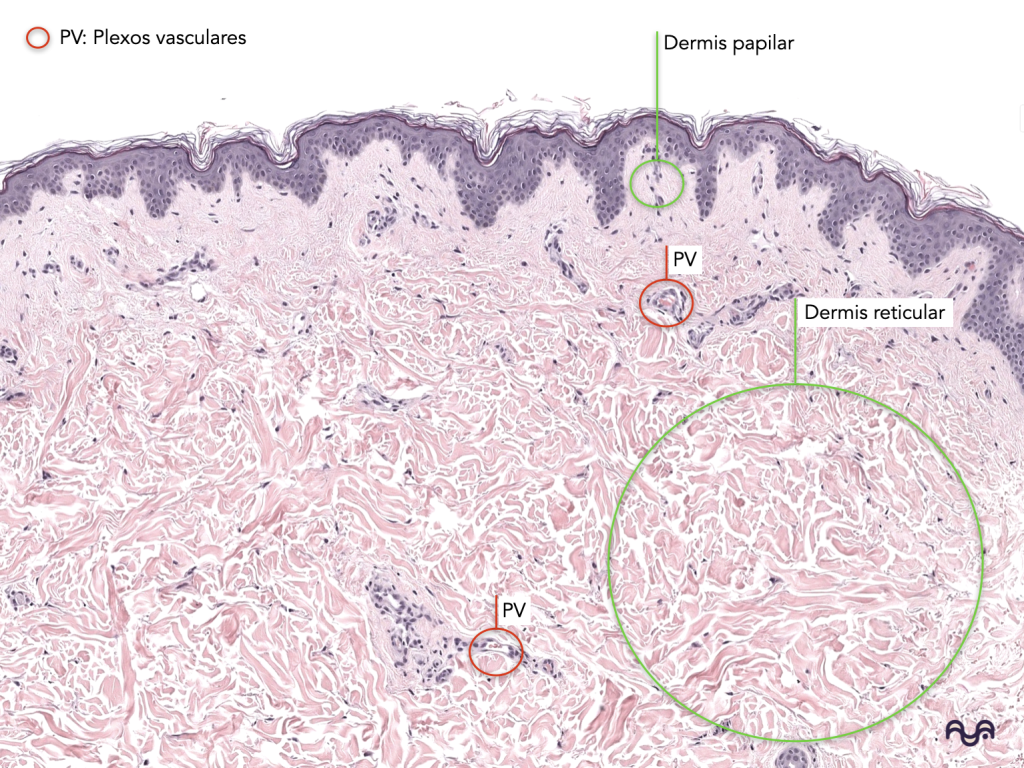
La dermis se divide en papilar (tejido conectivo laxo, más vascular, con papilas) y reticular (tejido conectivo denso irregular, con haces gruesos de colágeno). Brown 2022
-
En dermis papilar puedes encontrar corpúsculos de Meissner (tacto fino) en piel glabra; en dermis profunda/hipodermis, corpúsculos de Pacini (vibración/presión). Piccinin 2023 Brown 2022
-
Melanocitos (origen: cresta neural) viven sobre todo en la capa basal y transfieren melanosomas a queratinocitos. Huang 2024
-
Células de Langerhans (linaje mieloide) residen sobre todo en estrato espinoso, y son centinelas inmunológicas a nivel epidérmico. Igyártó 2013
-
Células de Merkel (forman complejos con aferencias para tacto discriminativo; suelen ubicarse en epidermis basal/“touch domes”. Woo 2015
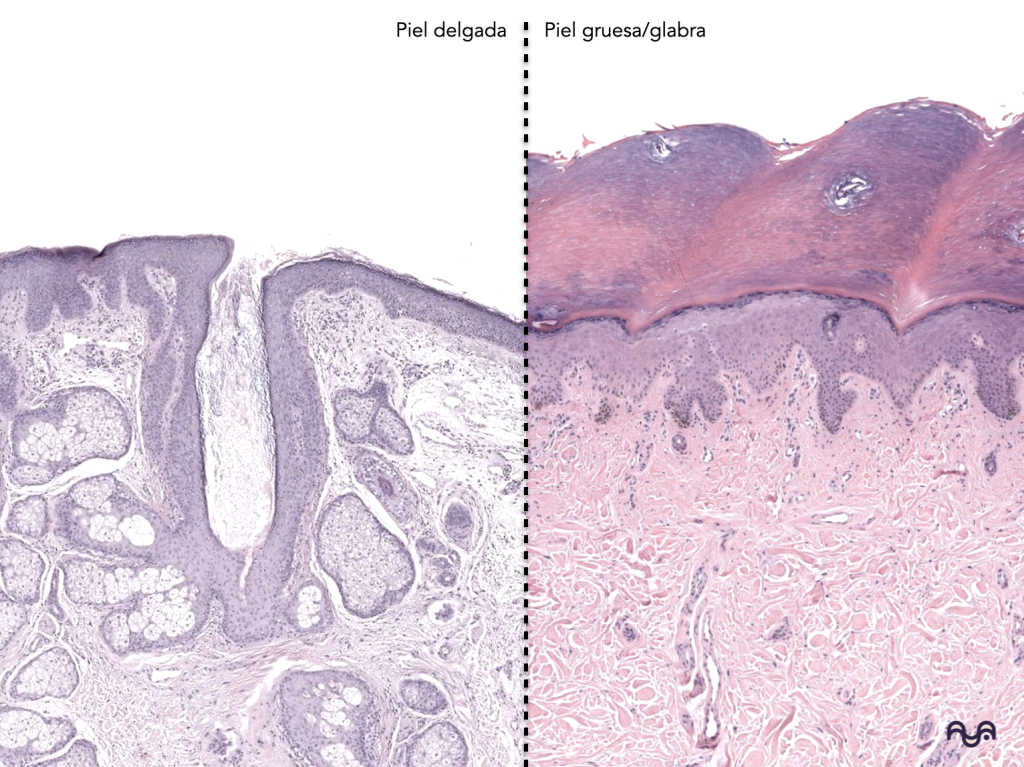
La piel gruesa: estrato córneo muy desarrollado, lúcido presente, sin folículos pilosos ni glándulas sebáceas, con muchas ecrinas. Lopez-Ojeda 2022
La piel delgada: estrato córneo más fino, con folículos y unidad pilosebácea variable según sitio. Agarwal 2023
Conceptos clave
1) Plan general (lo que estás viendo en el porta)
-
Epidermis: epitelio estratificado escamoso queratinizado, con renovación continua desde la capa basal hacia la superficie (diferenciación terminal/cornificación). Gutowska-Owsiak 2020
-
Dermis: tejido conectivo de origen mesenquimatoso (mesodermo), soporte mecánico, inmunidad y reparación; matriz extracelular rica en colágeno/elastina y “ground substance”. Brown 2022
-
Hipodermis (tejido celular subcutáneo): lobulillos de adipocitos con septos fibrosos; amortiguación, reserva energética, aislamiento térmico, y funciones endocrinas del tejido adiposo. Yousef 2024 Kershaw 2004
2) Variación normal (por qué “no se ve igual” en todos los cortes)
-
Sitio anatómico: palmas/plantas (glabra) vs cuero cabelludo vs tronco.
-
Orientación del corte: perpendicular vs tangencial (artefactos).
-
Edad/fotoexposición: modifica grosor epidérmico, elastosis, densidad de anexos (concepto general; para correlación clínica futura).
-
Estado funcional del folículo: anágeno/catágeno/telógeno (cambia la morfología).
Presentación histológica de la piel normal (según su zona anatómica)
-
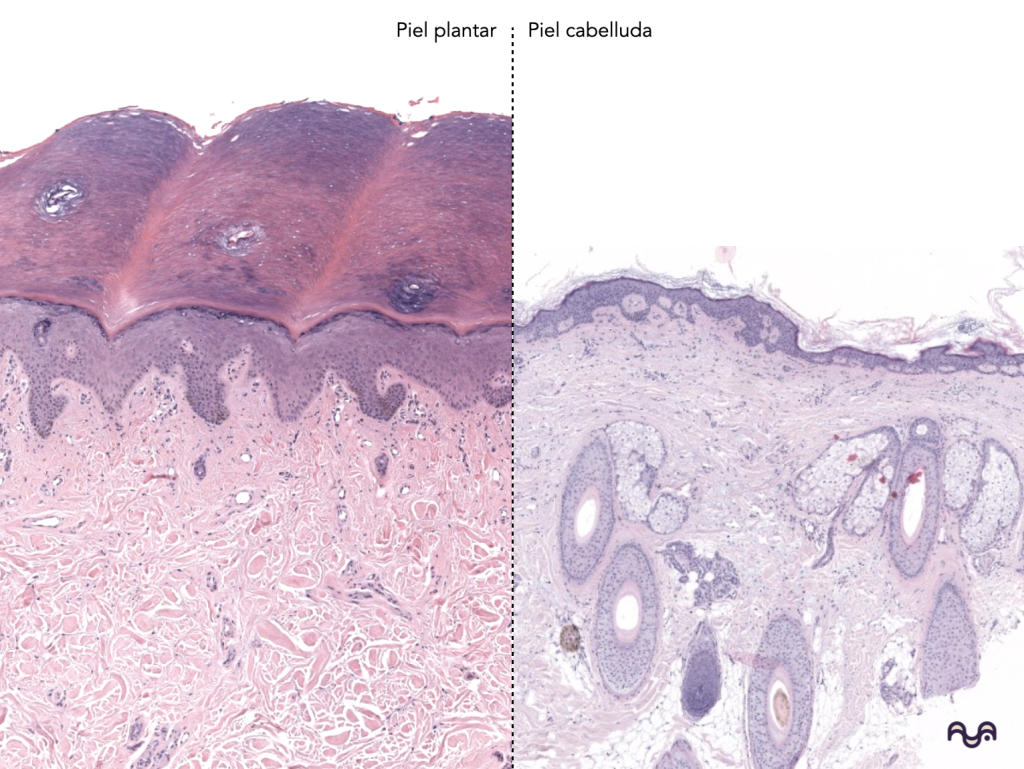
Piel glabra (palma/planta): epidermis muy gruesa, crestas epidérmicas prominentes, estrato córneo masivo, ecrinas abundantes; ausencia de unidad pilosebácea. Lopez-Ojeda 2022
-
Piel con pelo (la mayoría del cuerpo): folículos pilosos en distintos planos, glándulas sebáceas asociadas, músculo erector del pelo, ecrinas variables. Agarwal 2023
-
Dermis papilar: más “clara” y laxa cerca de la unión; capilares en asas dentro de papilas.
-
Dermis reticular: haces colágenos gruesos, más eosinofílicos, con anexos más profundos.
-
Perla: cuando te “pierdas”, vuelve a dos anclas visuales: (1) estrato córneo arriba; (2) grasa (si está) abajo. Todo lo demás se organiza entre esas referencias.
Ejercicio de lectura sistemática de la piel
Método “de arriba abajo” (método de 60–90 segundos)
Paso 1 — Baja magnificación (2×–4×): mapa general
-
Identifica la superficie: estrato córneo eosinofílico (a veces laminado).
-
Decide si es piel gruesa vs delgada:
-
-
gruesa: estrato córneo muy ancho + (posible) estrato lúcido + sin folículos;
-
delgada: estrato córneo fino + folículos con o sin pelo en el lumen. Kim 2023
-
-
Ubica anexos: folículos, glándulas, conductos, músculo erector. Agarwal 2023
-
Busca la hipodermis (si está): lobulillos adiposos con septos.
Paso 2 — Media magnificación (10×): epidermis por estratos
-
Basal: una hilera de células cúbicas/columnares bajas, con núcleos basófilos y citoplasma escaso. En este estrato es donde viven los melanocitos (no siempre obvios en H&E).
-
Espinoso: queratinocitos poligonales; “espinas” por desmosomas (artefacto de retracción que resalta puentes intercelulares).
-
Granuloso: gránulos de queratohialina basófilos; marca el “umbral” hacia cornificación.
-
Córneo: corneocitos anucleados; aplanados sobre su eje horizontal y de compactación variable (ortoqueratosis normal). Gutowska-Owsiak 2020
Paso 3 — La unión dermoepidérmica (la línea crítica)
-
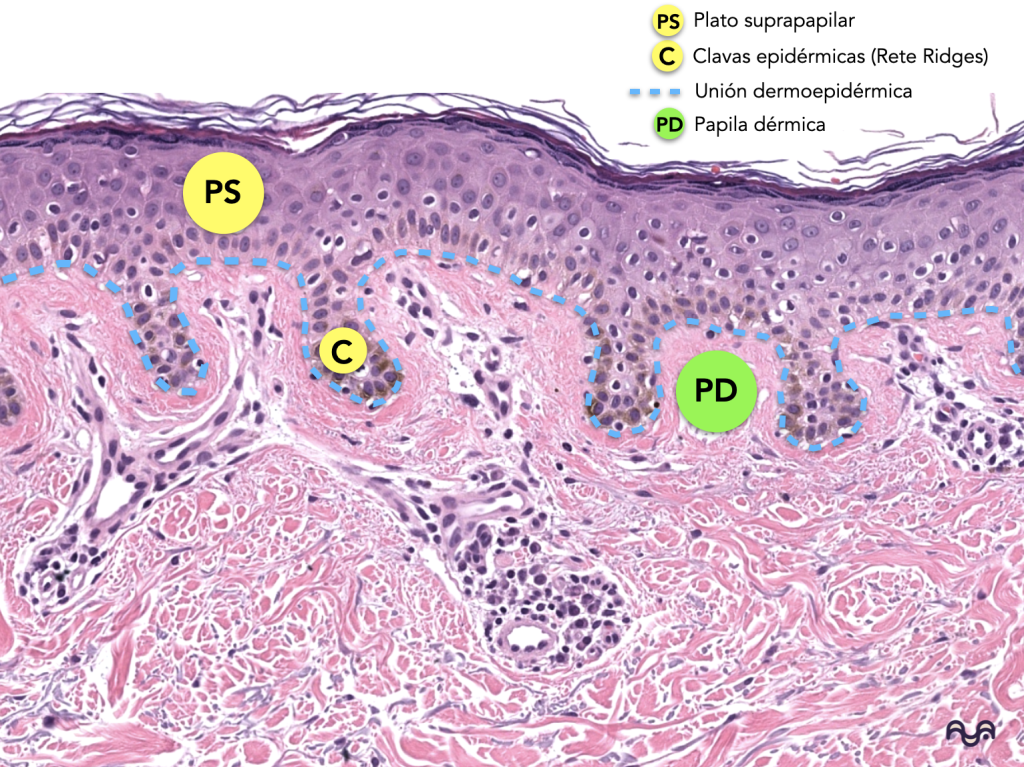
En H&E se ve como un contorno ondulado: crestas epidérmicas (rete ridges) que bajan y papilas dérmicas que suben.
-
Conceptualmente, ahí está la zona de membrana basal: laminina-332 y colágeno IV forman redes; el perlecano contribuye a la organización; los hemidesmosomas integran el anclaje del queratinocito basal. Kiritsi 2013 Behrens 2012 Walko 2014
Paso 4 — Dermis: papilar vs reticular
-
Papilar: tejido conectivo más laxo, más celular y vascular; papilas; posible Meissner en piel glabra. Brown 2022
-
Reticular: haces gruesos de colágeno (TC denso irregular), menos células aparentes, anexos más profundos.
Paso 5 — Hipodermis
-
Adipocitos uniloculares: citoplasma “vacío” (lípido extraído) con núcleo periférico; septos con vasos/nervios. Yousef 2024
Diferenciales útiles (cuando dudas si “es piel”)
-
Mucosa escamosa no queratinizada: ausencia de estrato córneo verdadero.
-
Piel vs cuero cabelludo: densidad folicular alta y unidades pilosebáceas prominentes.
-
Piel glabra vs delgada: ausencia/presencia de folículos y sebáceas.
Pitfalls (errores típicos)
-
Corte tangencial: puede simular acantosis/atrofia; confirma con el patrón global en baja magnificación.
-
Retracción: espacios en la unión o entre queratinocitos pueden parecer “espongiosis” si no valoras el contexto.
-
Planos del folículo: un folículo en transversal puede parecer “quiste”; busca el resto de la unidad y repetición del patrón.
-
Confundir estrato lúcido con “córneo compacto”: el lúcido es una banda pálida entre granuloso y córneo, típica de piel gruesa. Kim 2023
-
Llamar “glándula” a cualquier estructura tubular: distingue conducto ecrino (más oscuro, epitelio biestratificado) de porción secretora (células más claras/variadas y mioepiteliales). Yousef 2023
-
Pensar que “sin grasa = no es piel”: hay biopsias superficiales sin hipodermis; busca anexos y dermis reticular.
Lecturas recomendadas
Esenciales
Para profundizar
Bibliografía y fuentes
-
Yousef H, Alhajj M, Fakoya AO, Sharma S. Anatomy, Skin (Integument), Epidermis. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan–. Actualizado: 8 Jun 2024. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK470464/
-
Yousef H, Miao JH, Alhajj M, Badri T. Histology, Skin Appendages. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan–. Actualizado: 24 Abr 2023. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK482237/
-
Brown TM, Krishnamurthy K. Histology, Hair and Follicle. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan–. Actualizado: 1 May 2023. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK532929/
-
Piccinin MA, Miao JH, Schwartz J. Histology, Meissner Corpuscle. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan–. Actualizado: 6 Mar 2023. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK518980/
-
Patel BC, Treister AD, McCausland C, Lio PA, Jozsa F. Anatomy, Skin, Sudoriferous Gland. In: StatPearls[Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan–. Actualizado: 24 Abr 2023. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK513244/
-
Freeman SC, Malik A, Basit H. Physiology, Exocrine Gland. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan–. Actualizado: 26 Sep 2022. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK542322/
-
Gutowska-Owsiak D, et al. Addressing Differentiation in Live Human Keratinocytes by Assessment of Membrane Packing Order. Front Cell Dev Biol. 2020;8:573230. doi:10.3389/fcell.2020.573230. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC7609878/
-
Bikle DD, Xie Z, Tu C-L. Calcium regulation of keratinocyte differentiation. Expert Rev Endocrinol Metab. 2012;7(4):461–472. doi:10.1586/eem.12.34. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC3491811/
-
Del Rosso JQ, et al. Understanding the Epidermal Barrier in Healthy and Compromised Skin: Clinically Relevant Information for the Dermatology Practitioner. Proceedings of an Expert Panel Roundtable Meeting. J Clin Aesthet Dermatol. 2016;9(4 Suppl 1):S2–S8. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC5608132/
-
Kiritsi D, Has C, Bruckner-Tuderman L. Laminin 332 in junctional epidermolysis bullosa. Cell Adh Migr. 2013;7(1):135–141. doi:10.4161/cam.22418. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC3544777/
-
Behrens DT, et al. The Epidermal Basement Membrane Is a Composite of Separate Laminin- or Collagen IV-containing Networks Connected by Aggregated Perlecan, but Not by Nidogens. J Biol Chem. 2012;287(22):18700–18709. doi:10.1074/jbc.M111.336073. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC3365761/
-
Walko G, Castañón MJ, Wiche G. Molecular architecture and function of the hemidesmosome. Cell Tissue Res. 2014;360(2):363–378. doi:10.1007/s00441-014-2061-z. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC4544487/
-
Goletz S, Zillikens D, Schmidt E. Structural proteins of the dermal-epidermal junction targeted by autoantibodies in pemphigoid diseases. Exp Dermatol. 2017;26(12):1154–1162. doi:10.1111/exd.13446. Disponible en: https://pubmed.ncbi.nlm.nih.gov/28887824/
-
Villone D, et al. Supramolecular interactions in the dermo-epidermal junction zone: anchoring fibril-collagen VII tightly binds to banded collagen fibrils. J Biol Chem. 2008;283(36):24506–24513. doi:10.1074/jbc.M802415200. Disponible en: https://pubmed.ncbi.nlm.nih.gov/18599485/
-
Niemann C, Horsley V. Development and homeostasis of the sebaceous gland. Semin Cell Dev Biol. 2012;23(8):928–936. doi:10.1016/j.semcdb.2012.08.010. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC5595243/
-
Cui C-Y, Schlessinger D. Eccrine sweat gland development and sweat secretion. Exp Dermatol. 2015;24(9):644–650. doi:10.1111/exd.12773. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC5508982/
-
Igyártó BZ, Kaplan DH. Antigen presentation by Langerhans cells. Curr Opin Immunol. 2013;25(1):115–119. doi:10.1016/j.coi.2012.11.007. Disponible en: https://pubmed.ncbi.nlm.nih.gov/23246038/
-
Woo S-H, Lumpkin EA, Patapoutian A. Merkel cells and neurons keep in touch. Trends Cell Biol. 2015;25(2):74–81. doi:10.1016/j.tcb.2014.10.003. Disponible en: https://pubmed.ncbi.nlm.nih.gov/25480024/
-
Bento-Lopes L, et al. Melanin’s Journey from Melanocytes to Keratinocytes: Uncovering the Molecular Mechanisms of Melanin Transfer and Processing. Int J Mol Sci. 2023;24(14):11289. doi:10.3390/ijms241411289. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC10379423/
-
Vandamme N, et al. From neural crest cells to melanocytes: cellular plasticity during development and beyond. Cell Mol Life Sci. 2019;76(10):1919–1934. doi:10.1007/s00018-019-03049-w. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC11105195/
-
Huang L, Zuo Y, Li S, Li C. Melanocyte stem cells in the skin: Origin, biological characteristics, homeostatic maintenance and therapeutic potential. Clin Transl Med. 2024;14(5):e1720. doi:10.1002/ctm2.1720. Disponible en: https://pubmed.ncbi.nlm.nih.gov/38778457/
-
Kershaw EE, Flier JS. Adipose tissue as an endocrine organ. J Clin Endocrinol Metab. 2004;89(6):2548–2556. doi:10.1210/jc.2004-0395. Disponible en: https://pubmed.ncbi.nlm.nih.gov/15181022/



 |
|